A tisztánlátás kedvéért egy rövid ismétléssel kezdem. Az LDL (a leginkább koleszterinben gazdag) lipoporotein. Ha túl sok időt tölt a keringésben, hajlamossá válik az oxidációra.
Az LDL köpeny részében lévő többszörösen telítetlen zsírsavakat szabadgyökök károsítják, majd a folyamat tovább terjedésével a köpeny fehérjéi is sérülnek, végül a mag zsírsav részecskéi is.
Mi történik az oxidált LDL részecskével?
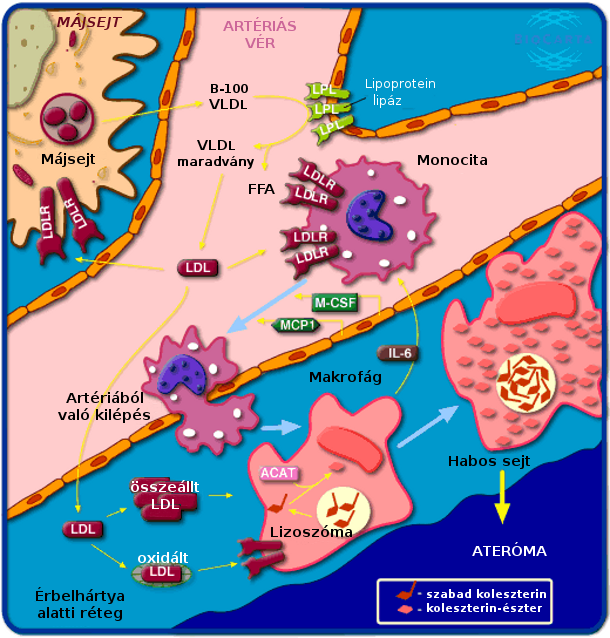 Miután az LDL oxidálódik, képessé válik a verőér falába történő invázióra, főleg azokon a területen, ahol a véráramlás örvénylővé válik (turbulencia). Ezek a pontok főként ott találhatóak, ahol az érrendszer nem egyenes vagy elágazik. Ezek a területek a nagy molekulák számára könnyebben átjárhatóak. Az oxidált LDL részecskék magukhoz vonzzák az immunrendszer részeként működő, az érfal épségéért felelős fehérvérsejteket (monocyták/makrofágok). Ez a mozzanat az első lépcsője annak a gyulladásos folyamatsornak, amely végül az instabil érfali plakk kialakulását eredményezi. Ez az alapja az “oxidált LDL okozta érelmeszesedés” elméletnek.
Miután az LDL oxidálódik, képessé válik a verőér falába történő invázióra, főleg azokon a területen, ahol a véráramlás örvénylővé válik (turbulencia). Ezek a pontok főként ott találhatóak, ahol az érrendszer nem egyenes vagy elágazik. Ezek a területek a nagy molekulák számára könnyebben átjárhatóak. Az oxidált LDL részecskék magukhoz vonzzák az immunrendszer részeként működő, az érfal épségéért felelős fehérvérsejteket (monocyták/makrofágok). Ez a mozzanat az első lépcsője annak a gyulladásos folyamatsornak, amely végül az instabil érfali plakk kialakulását eredményezi. Ez az alapja az “oxidált LDL okozta érelmeszesedés” elméletnek.
Mit csinál a HDL?
Számos közlemény foglalkozik a „fordított koleszterin szállítás” mechanizmusával, mely szerint a HDL kivonja a verőér falából a koleszterint, de a HDL molekulának ezen túlmenően érvédő szerepet is tulajdonítanak antioxidáns és gyulladás-csökkentő képességei révén.
Mi az a Lipoprotein “a” vagy Lp(a)?
A Lipoprotein “a”, rövidítve Lp(a), gyakorlatilag az LDL egy kisebb származéka. A Lp(a) a verőerek plakkjaiban található, az érelmeszesedés erős, független kockázati tényezője. A 80-as évek végén közzétett feltételezés szerint az Lp(a) a vér alvadását gátló egyik enzim blokkolásával elősegíti a vérrögképződést.
A legújabb kutatások szerint gyakorlatilag az összes, oxidált foszfolipidet tartalmazó LDL kapcsolatban van az Lp(a)-val. Ezen felül az oxidált LDL közvetlenül oxidált foszfolipideket ad át a köpeny részből az Lp(a) molekulának. Így az Lp(a) az LDL-köpeny oxidációs állapot-jelzőjének tartható, bár az is valószínű, hogy az Lp(a) a sejtek hártyájából is vesz fel oxidált foszfolipid molekulákat (például a verőerek belső falának sejtjeiből).
Az LDL-Receptor (LDL-R) jelentősége az érbetegség kialakulásában
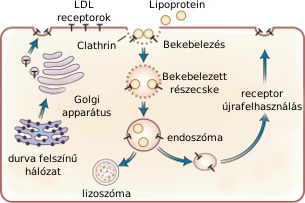
A korábbi bejegyzésekben láttuk, hogy minél tovább marad az LDL a keringésben és minél később kerül eltávolításra az LDL-receptor segítségével, annál nagyobb az esélye, hogy oxidatív átalakuláson megy át és plakk-képző tulajdonságúvá válik. Ezt is figyelembe véve az érelmeszesedés folyamatának hátterében TÖBB mechanizmus állhat:
-
A túl sok LDL a vérkeringésben egyszerűen „túltölti” a finoman szabályozott lipoprotein körforgást. Ezt gyakorlatilag elhízásban és az úgynevezett metabolikus tünetegyüttesben látjuk, ahol a zsírszövet tartós zsírsav kibocsátása miatt a vér triglicerid-szintje megemelkedik; magas LDL, VLDL, IDL szintek mellett alacsony HDL jellemző a kórfolyamatra.
-
A keringési rendszer magas oxidatív terhelése: pl. dohányosokban, elhízásban és metabolikus tünetegyüttesben, mozgásszegény életmód, érrendszeri kondíció hiánya esetén, TRANSZ-zsírsavakban és oxidált többszörösen telítetlen omega-6 zsírsavakban gazdag étrend kapcsán; omega-3 zsírokban, természetes antioxidánsokban szegény étrendnél; magas vérnyomásban és cukorbetegségben szenvedőknél.
-
A májsejtek alacsony LDL-receptor száma vagy alacsony aktivitása (öröklött magas koleszterinszint és az úgynevezett PCSK9 gén eltérései). Ha az LDL-receptor működése zavart szenved, lelassul az LDL eltávolítása a keringésből, ezzel több ideig lesz kitéve az oxidatív hatásoknak és hosszabb ideig képes az érfalkárosító-hatás kifejtésére. Az LDL felületén lévő apoB100 fehérje hibás, károsodott szerkezete is csökkenti az LDL-receptor hatékonyságát annak ellenére, hogy az LDL-receptor szerkezete normális. Ellenkezőleg, a PCSK9 gén olyan eltérései, amelyek az LDL-receptorok számának növekedéséhez vezetnek, jelentősen csökkentik az érbetegség kockázatát.
-
Az LDL termelődését más hormonrendszerek is befolyásolják és hozzájárulnak az LDL szint emelkedéséhez és oxidációjához. Alacsony pajzsmirigy hormon szint, magas ösztrogén (női hormon) szint (elhízás/metabolikus tünetegyüttes) és emelkedett mellékvesekéreg-hormon szint is társulhat magas LDL szinttel.
Összefoglalva:
-
Láthatjuk, hogy az ÖSSZ-koleszterin szint mérése önmagában gyenge előrejelzője a verőérbetegség kialakulásának.
-
Világos, hogy az LDL a meghatározó molekulája az érelmeszesedés elindulásának. Emellett az immunsejtek természetes reakciója, hogy az érfal épségét biztosítsák, egy gyulladásos folyamatot indít el, amely az érfali plakk kialakulásához és instabilitásához vezet.
-
Egyértelmű, hogy a koleszterin FŐ szállítója az LDL molekula, az LDL-koleszterin magas szintje igen erős jelzője az érbetegségnek.
-
Ezek a jelenségek kiegészülhetnek alacsony HDL szinttel járó kórállapotokkal.
-
A magas triglicerid szint általában magas VLDL és IDL szinttel jár, bár ezeket rutinszerűen nem mérjük. Magas triglicerid szint esetén gyakran látunk alacsony HDL szinteket, és ha a teljes koleszterinszintből kivonjuk a HDL értékét, megkapjuk a „nem-HDL” frakciót. Ez jól képviseli az ÖSSZES plakk-képző képességű lipoprotein szintjét és így szintén jó előrejelzője a verőérbetegségeknek.
-
Minél inkább oxidálódik az LDL, annál kisebbé és sűrűbbé válik (úgynevezett B-típusú LDL), szemben az A-típusú LDL molekulával (nem oxidált, lebegőképes, nagy bolyhos LDL), ez utóbbi csak minimális plakk-képző tulajdonságú, míg a B-típus erősen plakk-képző típus.
-
Különösen JÓ értékelési lehetőség a „teljes” ér-rizikó meghatározására az apoB fehérje szintjének mérése, mert ez a fehérje az összes káros hatású lipoproteinben megtalálható (LDL + VLDL + IDL).
A megismert mechanizmusokból adódik, hogy miként lehet ezeket a jelenségeket gyógyszeresen befolyásolni. Ezekről későbbi bejegyzésekben részletesen szó lesz, itt rövid összefoglalását adom a lehetőségeknek:
-
A statinok a májsejtek koleszterin-szintézisének meghatározó enzimét gátolják, ezáltal csökkentik a májsejtek koleszterin tartalmát. A májsejtek ezt a folyamatot úgy érzékelik, hogy a szervezetben kevés a koleszterin, ezért megnövelik a sejtfelszíni LDL-receptorok számát. Több koleszterint vonnak ki így a keringésből és megnövelik a májsejt koleszterin tartalmát. A folyamat eredményeként a keringő LDL molekulák száma csökken, a maradék kevesebb ideig tartózkodik a vérkeringésben, így kevesebb ideig lesz kitéve az oxidatív károsodásnak.
-
A PCSK9 gátlók szintén növelik a májsejtek felszínén az LDL-receptorok számát, alacsonyabb vér LDL szintet eredményezve csökkentik az érbetegség kockázatát.
-
Az ezetimib nevű molekula a bélhámsejtek felszínén gátolja a koleszterin felszívódását, így csökkenti a kilomikronokba jutó koleszterin és koleszterin-észter mennyiséget, ez végül kevesebb LDL képződéséhez vezet.
 Follow
Follow